Podczas niedawnej konferencji Centrum Badań Przedklinicznych i Technologii (CEPT) mówił pan o nicieniu. Skąd nicień na spotkaniu poświęconemu innowacyjnej biomedycynie?
W latach 60. i 70. ubiegłego wieku Sydney Brenner uczynił go modelowym systemem do badania budowy układu nerwowego. Stworzył całą dziedzinę nauki, na początku w genetyce, a potem w biologii rozwoju, biochemii i farmakologii.
Nicień, czyli?
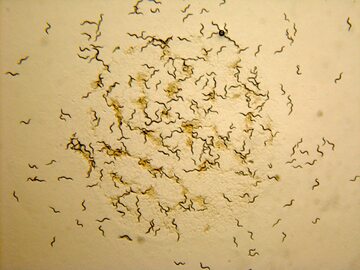
Nicień glebowy, o wdzięcznej nazwie Caenorhabditis elegans (C. elegans), potocznie nazywany robakiem, żyje w glebach w cieplejszym klimacie, na przykład w Europie Zachodniej; u nas jest mu trochę za zimno. Ma około milimetra długości, 959 komórek, z czego 302 to neurony.
My, ludzie, mamy około 20 tysięcy genów kodujących białka. Robaki też mają około 20 tys. genów, co niektórzy mogą uważać za trochę wstydliwe dla nas. Robaki mają wszystkie ważne tkanki: skórę, układ nerwowy, rozrodczy, wydalniczy, trawienny – są pod tym względem bardzo podobne do nas. C. elegans to taki malutki model człowieka. Jest to też pierwszy organizm wyższy, którego genom został zsekwencjonowany; poznaliśmy wszystkie jego geny.
Co ma to wspólnego z medycyną?
Dzięki łatwości manipulacji genetycznych możemy w robakach tworzyć modele chorób ludzkich. Na przykład dzięki metodzie CRISPR, za którą niedawno przyznano Nagrodę Nobla, możemy łatwo zmienić pojedynczy nukleotyd (podstawowa jednostka budowy DNA i RNA – red.) w genomie robaka. Stworzenie zmienionego genetycznie robaka zajmuje zaledwie kilka tygodni.
Uzyskujemy tę samą mutację, która wywołuje jakąś chorobę u człowieka?
Na przykład. Ja zrobiłem to, próbując modelować ludzką chorobę związaną z mutacją w genie PACS2, powodującą neuropatię rozwojową i padaczkową. Zmieniłem pojedynczy nukleotyd, który powoduje pojedynczą mutację aminokwasów w robaczym odpowiedniku ludzkiego genu PACS2. Na świecie jest 60 pacjentów z chorobą spowodowaną tą mutacją.
W Polsce jest rodzina, w której urodziło się takie chore dziecko. Jego rodzice założyli i prowadzą fundację naukową PACS2 Research Foundation. Finansują badania w różnych obszarach, w tym moje na robakach, by znaleźć pomoc dla swojego dziecka, a także wszystkich innych pacjentów z tą mutacją. To nie jest coś, za co Big Pharma chciałaby zapłacić, bo Big Pharma musi zarobić. Na świecie jest bardzo wiele fundacji finansujących badania nad chorobami rzadkimi, ale w Polsce filantropia w badaniach naukowych prawie nie istnieje.
Opracowanie nowego leku kosztuje niebotyczne pieniądze…
Koszty jednego leku – od wytypowania celu leku do wprowadzenia cząsteczki jako leku to średnio 2 mld dolarów, a cały proces trwa 15 lat. Podzielmy te 2 mld dolarów przez 60 pacjentów. Kogo będzie stać na taki lek?
Jak wszczepienie mutacji do nicienia pomaga w znalezieniu sposobu leczenia choroby rzadkiej?
Jeżeli w robaku możemy wywołać „chorobę”, to możemy poszukać leku na tę chorobę, traktując zmutowanego robaka dostępnymi lekami. W badaniach wykorzystujemy leki dopuszczone przez FDA (amerykańska Agencja Żywności i Leków), bo jeżeli jest to lek dopuszczony do obrotu, to nie trzeba robić badań klinicznych lub trzeba ich zrobić znacznie mniej.
Badania na robakach pomagają w zrozumieniu patogenezy choroby?
Możemy zbadać i zrozumieć patogenezę choroby, wykonując model w nicieniu. Możemy też szukać leku. Te rzeczy wbrew pozorom są zupełnie niezależne od siebie. Możemy zrozumieć patogenezę choroby, ale to bardzo rzadko pomaga w znalezieniu leków. Jest naprawdę niewiele leków, które były wymyślone w ten sposób. Przykładem jest imatynib, jeden z leków stosowanych w białaczce limfoblastycznej. Większość leków odkryto przez przypadek. Bo tak naprawdę nie muszę znać patogenezy choroby, wystarczy, że ją odwrócę. Jeżeli będę miał dobry sposób na sprawdzanie i odróżnienie robaków chorych na chorobę PACS2 z tymi, które nie są chore, to wtedy mogę sprawdzać kolekcję leków.

Na chybił trafił?
Tak robią firmy farmaceutyczne. Przebadanie 2 mln cząstek zajmuje firmie 24 godziny w badaniach in vitro. Tylko co potem? Jeśli to samo się zrobi na robakach i zacznie się od kilku tysięcy leków, które są już dopuszczone do użytku albo są w końcowej fazie badań klinicznych, to można przeskoczyć bardzo dużo etapów.
Mutujemy robaka i sprawdzany, czy działają na niego te leki, które zostały zarejestrowane?
Tak. Oczywiście to nie znaczy, że się uda. Jeśli się jednak uda, to mamy bardzo szybką drogę do tego, żeby użyć tego leku.
Takie operacje możemy przeprowadzać nie tylko na robakach. Można je robić również na drożdżach. U nas w instytucie prof. Róża Kucharczyk, wykorzystując ten pomysł – tylko w drożdżach, znalazła lek na chorobę mitochondrialną związaną z mutacjami w genie ATP6 – syndrom NARP (neuropatia, ataksja i barwnikowe zwyrodnienie siatkówki). W drożdżach można manipulować genomem mitochondrialnym. Prof. Kucharczyk sprawdziła na drożdżach, czy da się zmienić fenotyp (zestaw cech) drożdżowy mutacji powodującej neuropatię, i okazało się, że jeden z leków na malarię, chlorheksydyna, odwraca ten fenotyp w drożdżach, co potem zostało potwierdzone w komórkach ludzkich.
I ten lek został zastosowany?
O ile wiem – nie. Trzeba znaleźć lekarza, który by zechciał to wykorzystać u pacjenta z chorobą ultrarzadką. Natomiast nikt by się nie spodziewał, że drożdże i lek na malarię pomogą na neuropatię.
Czy robaki już pomogły w znalezieniu nowych zastosowań starych leków?
Wiele takich modeli jest rozwijanych. Dzięki odkryciu tzw. zjawiska interferencji RNA – badania przeprowadzano na robakach – udaje się znajdować nowe leki. I za to odkrycie był również Nobel – dla Andy Fire’a i Craiga Mello. Mówiąc w dużym uproszczeniu wymyślili oni technikę, która służy do wyciszania aktywności specyficznych genów. Rok temu było już 5 leków dopuszczanych przez FDA, które powstały dzięki tej technice, a kilkadziesiąt kolejnych przechodzi badania kliniczne.
Na jakie choroby są te leki?
Neurodegeneracyjne, nowotworowe, wirusowe i cukrzycę.
My dzięki robakom znaleźliśmy nową klasę antybiotyków. Właściwie to ich nie szukaliśmy. Rozmawiając przy kawie z prof. Wojciechem Balem, doszliśmy do wniosku, że substancje, których on używa do badania wiązania metali, mogłyby zadziałać jako antybiotyki, ponieważ mogłyby wprowadzać jony miedzi do bakterii. Wziąłem więc te związki, które mój rozmówca trzymał w lodówce, i potraktowałem nimi robaki w modelu infekcyjnym robaka. Okazało się, że jeden z tych związków działa.
Jak poznać, że jakaś cząsteczka działa na robaka?
Jeżeli robimy badania farmakologiczne robaka, to mamy odpowiedź zerojedynkową. Jeżeli związek nie wyleczy choroby, to robak zdycha. Jeżeli jest to związek toksyczny dla robaka – robak zdycha. Zadziałają jedynie takie cząsteczki, które nie będą zatruwać robaka, ale będą truć bakterie i jeszcze do tego będą się odpowiednio rozprowadzać w robaku. Tak więc w jednym badaniu można odpowiedzieć na wszystkie pytania.
Wprowadził pan do robaka związek mający powinowactwo do miedzi i odkrył potencjalnie nową klasę antybiotyków. I co dalej? Są szanse, że ta substancja zostanie zarejestrowana?
Uznaliśmy, że to będzie działać, że warto te badania kontynuować. Zrobiliśmy badania około 200 podobnych substancji i we współpracy z Uniwersytetem Medycznym w Białymstoku udało nam się udowodnić, że nasz związek zabija między innymi lekooporną bakterie Klebsiella pneumoniae.
Słynną superbakterię, nazywaną New Delhi, oporną na wszystkie antybiotyki?
Tak.
Jednak jeśli chodzi o komercjalizację tego odkrycia, to nie ma najmniejszych szans. Założyliśmy start-up, który miał na celu komercjalizację, ale nic z tego nie wyszło. Zresztą wszystkie duże firmy farmaceutyczne zarzuciły swoje programy antybiotykowe, nikt nie rozwija antybiotyków.
Dlaczego?
Problem z antybiotykami jest taki, że jeśli nie będziemy ostrożni w ich używaniu, pojawia się antybiotykooporność. A prawie cała lekooporność bierze się z hodowli zwierzęcej. Przemysł spożywczy zużywa rocznie 5 tys. ton kolistyny. To antybiotyk ostatniej szansy, dość toksyczny dla ludzi, stosowany wtedy, gdy już nic innego nie działa, kiedy nie działa nawet wankomycyna. Ten antybiotyk w Europie jest podawany tylko w szpitalach zakaźnych. W Chinach, ale też we Polsce, używa się go przy hodowli drobiu i trzody chlewnej. Dlatego już parę lat temu pojawiała się oporność na ten antybiotyk.
To dlaczego nie ma szansy na komercjalizację waszego antybiotyku?
Bo to się nie opłaca. Firmy farmaceutyczne mówią rządom: „Dajcie nam pieniądze, żeby opracować antybiotyk, bo jeżeli my to zrobimy za własne pieniądze, to ktoś zacznie go stosować przy hodowli kurczaków i za trzy miesiące pojawi się na niego oporność, i nic na tym nie zarobimy”. Ostatnią nadzieją na rozwój antybiotyków są organizacje non-profit, które finansują z prywatnych pieniędzy rozwój antybiotyków.
Czy jest jeszcze jakieś inne zastosowane robaków?
C. elegans jest też wykorzystywany jako model badania nicieni pasożytniczych. Nie są one może problemem w naszych szerokościach geograficznych, ale przez ocieplenie klimatu niedługo będą. Na świecie ponad miliard ludzi jest zarażonych którymś z nicieni pasożytniczych, a sto tysięcy umiera rocznie z tego powodu. Straty w rolnictwie z powodu nicieni pasożytniczych roślin to ponad 150 miliardów dolarów rocznie.
Robaki mogą być również wykorzystywane w badaniu toksyczności substancji chemicznych. Unia Europejska wydała dyrektywę REACH dotyczącą badania związków chemicznych. Z 35000 związków tzw. istotnych w Unii Europejskiej zaledwie 4000 zostało przebadanych toksykologicznie – więc tak naprawdę nie wiemy, w jakim otoczeniu żyjemy.
Te badania przeprowadza się na zwierzętach, ale równie dobrze na te pytania mogą odpowiedzieć badania na robakach. Badania toksykologiczne kosztują 2 miliardy euro i życie milionów zwierząt rocznie. Badania na robakach są dużo prostsze, w dodatku bardzo szybkie i bardzo tanie. Zaletą robaków jest to, że na nich możemy badać toksykologię rozwojową. Ponieważ cykl życia robaka trwa trzy dni, to możemy sprawdzić, czy pod wpływem danego związku nie dzieje się coś złego w rozwoju embrionalnym. Możemy też badać neurotoksykologię – czyli jak dana substancja działa na układ nerwowy.
Dr Krzysztof Drabikowski, Instytut Biochemii i Biofizyki PAN. Ukończył studia magisterskie na Wydziale Biologii UW. Doktorat obronił we Friedrich Miescher Institute for Biomedical Research w Bazylei, Staże podoktorskie odbywał w FMI i The Scripps Research Institute, La Jolla California, USA. Assistant professor na University we Freiburgu, Niemcy. Aktualnie zatrudniony w IBB PAN. Współzałożyciel i prezes start-upu zajmującego się poszukiwaniem nowych antybiotyków, również przy użyciu robaków C. elegans.
Autor: Dorota Bardzińska